Uwolnij pełen potencjał swojego umysłu. Naukowo.


LEPSZA PAMIĘĆ

WYDŁUŻONA KONCENTRACJA

SZYBSZE MYŚLENIE



Zobacz, czym jest oraz jak powstał Science Care Pamięć i Koncentracja™
Prawdziwa historia


Efekty stosowania:

Lepsza pamięć i zapamiętywanie
Nasz suplement zawiera składniki aktywne, które mają dowiedzione działanie polepszające funkcjonowanie różnych obszarów pamięci.

Głęboka koncentracja i precyzyjne skupienie
Zobacz, jak to jest, gdy jesteś w stanie skoncentrować się na swoich zadaniach znacznie dłużej niż zwykle i szybciej kończyć wszystko, co sobie zaplanowałeś.

Wzrost kreatywności i szybsze myślenie
Dzięki składnikom polepszającym komunikację między neuronami zaczniesz lepiej kojarzyć fakty, rozwiązywać problemy i wpadać na bardziej kreatywne rozwiązania.
Dla kogo?
Science Care Pamięć i Koncentracja™ to produkt wspomagający pracę mózgu przeznaczony dla osób powyżej 18 roku życia — zarówno dla mężczyzn, jak i kobiet.
Jest szczególnie przydatny u osób, dla których kluczowe jest wysokie skupienie, dobra pamięć, szybkie przetwarzanie informacji i podejmowanie trafnych decyzji (np. pracownicy umysłowi, menedżerowie, przedsiębiorcy, programiści, startupowcy, inwestorzy czy sportowcy).
Sprawdzi się także u osób, które chcą w naturalny sposób szybciej się uczyć, poprawić pamięć lub po prostu wykorzystać w pełni potencjał swojego umysłu


Roślinny skład w pełni opartyna badaniach naukowych
Gdy przekopywaliśmy się przez naukowe bazy danych szukając substancji, które polepszają pamięć i koncentrację, mieliśmy dwa kryteria:
- Właściwości tych substancji muszą być potwierdzone przez wiele zróżnicowanych eksperymentów. To muszą być substancje, co do których nauka nie ma żadnych wątpliwości, że dają mierzalne efekty.
- Te substancje muszą być korzystne dla zdrowia przy długotrwałym stosowaniu.
Po przeanalizowaniu setek badań i metaanaliz, okazało się, że ze wszystkich substancji nasze kryteria najlepiej spełnia 5 ekstraktów roślinnych.


Czy wiesz, że: w bibliografii na końcu strony znajdziesz ponad 190 źródeł naukowych, które potwierdzają skuteczność składników suplementu.
Dlatego w każdej kapsułce znajdziesz tylko te ekstrakty - żadnych zbędnych wypełniaczy, konserwantów, barwników czy innych dodatków. Tylko to, co naprawdę działa:
Ashwagandha
łac. Withania somnifera
- Wspomaga pamięć i koncentrację [1] [2]
- Wspiera procesy uczenia się i przypominania sobie informacji [1-4]
- Przyczynia się do utrzymania optymalnej aktywności umysłowej i poznawczej [5-11]
- Jako adaptogen pomaga radzić sobie m.in. ze stresem i napięciem emocjonalnym [12-15] [30]
- Wspiera w okresach osłabienia, wyczerpania, zmęczenia [14-19]

Żeń-szeń amerykański i koreański
łac. Panax quinquefolius L., Panax ginseng
- Wspiera sprawność umysłu, poprawiając pamięć i koncentrację [37-44] [48]
- Pomaga w utrzymaniu dobrej sprawności poznawczej [39] [45-48]
- Przyczynia się do utrzymania optymalnej aktywności umysłowej również w okresach osłabienia, wyczerpania, zmęczenia i utraty koncentracji [48-51]
- Poprawia krążenie krwi, co pozytywnie wpływa na wydajność mózgu [52-55]
- Ginsenozydy zawarte w żeń-szeniu stymulują organizm w okresach, gdy potrzebna jest jego większa wydajność [43] [44] [53-57]
- Wzmacnia organizm oraz wspiera prawidłowe funkcjonowanie układu odpornościowego [58-65]

Różeniec górski
łac. Rhodiola rosea
- Wspomaga aktywność umysłową i umiejętności poznawcze [97-101] [135]
- Poprawia krążenie krwi, co pozytywnie wpływa na wydajność mózgu [102-106]
- Pomaga poprawić percepcję [100]
- Wspiera prawidłowe funkcjonowanie układu nerwowego [107-111]
- Wspomaga w okresach spadku wydajności [99] [112-118] [120]
- Jako adaptogen pomaga radzić sobie m.in. ze stresem i napięciem emocjonalnym [99] [100] [109] [112] [113] [118]
- Redukuje zmęczenie i bóle głowy wywołane stresem [116] [120-122]

Bakopa drobnolistna
łac. Bacopa monnieri
- Wykazuje pozytywny wpływ na ogólne funkcjonowanie mózgu [136-145]
- Wspomaga zdolność uczenia się, pamięć (zarówno krótko-, jak i długotrwałą) oraz koncentrację [146-160]
- Poprawia zdolności poznawcze i umiejętności zapamiętywania [160-172]
- Poprawia krążenie krwi, co przyczynia się do zwiększenia wydajności pracy mózgu [173-176]
- Wzmacnia układ nerwowy [160] [174] [177-180]
- Zawiera dużą ilość naturalnie występujących przeciwutleniaczy, które chronią komórki i tkanki mózgu przed uszkodzeniami oksydacyjnymi [181-185]

Tabela składników aktywnych

OPINIA EKSPERTA
Wsparcie naszego umysłu - zgodnie z naturą

Dobrze wiemy, jak szybkie tempo życia, wymagające zadania i natłok spraw do załatwienia odbijają się na naszym zdrowiu.
W konsekwencji czujemy się przytłoczeni, łatwiej się rozpraszamy, czy częściej wypada nam coś z głowy.
W składzie Science Care Pamięć i Koncentracja™ znalazły się bezpieczne naturalne składniki aktywne, które wspierają nasz mózg i pozwalają wykorzystać jego pełen potencjał. W środku kapsułki znajdziemy między innymi unikalny duet dwóch odmian żeń-szenia - koreańskiego i amerykańskiego. Dane literaturowe pokazują, że oba te żeń-szenie zawierają wyjątkowy dla siebie profil ginsenozydów, których dotąd wyizolowano i określono struktury kilkudziesięciu z nich. To właśnie te cząsteczki mają pozytywny wpływ na funkcje poznawcze naszego mózgu. Z badań naukowych wiemy na przykład, że przyjęcie żeń-szenia koreańskiego znacznie zwiększa sprawność w rozwiązywaniu testów oraz redukuje odczuwane podczas nich zmęczenie umysłowe.
Dodatkowo w dziennej dawce Science Care Pamięć i Koncentracja™ znajduje się najwyższa dopuszczona na rynku zawartość składników aktywnych pochodzących z ashwaghandy i różeńca górskiego (witanolidów i rozawin). To m.in. za tymi substancjami stoi szereg prozdrowotnych właściwości obu tych roślin.
Paweł Niewiarczuk
Dietetyk (Akademia Wychowania Fizycznego im. E. Piaseckiego w Poznaniu)


100%
składników naturalnego pochodzenia

Odpowiedni dla diety wegańskiej, wegetariańskiej, paleo
i keto

bez cukru

bez orzechów

bez kofeiny

bez glutenu

bez laktozy
Bezpieczeństwo?
Każdą partię badamy dwukrotnie.

Stworzyliśmy ten suplement w pierwszej kolejności dla siebie - sami spożywamy go każdego dnia.
Tak samo jak Ty - my też chcemy mieć pewność, że bierzemy tylko to, co najlepsze.
Dlatego każdą partię suplementu po wyprodukowaniu sprawdzamy dodatkowo drugi raz w zewnętrznym akredytowanym laboratorium J.S Hamilton.
Sprawdzamy, czy partia zawiera to, czego chcemy (np. odpowiednią ilość witanolidów pochodzących z ashwagandhy) oraz czy nie zawiera niczego, czego nie chcemy (np. bakterii, WWA czy metali ciężkich).
Podczas badań stosujemy się do najnowszych odkryć i wytycznych, dlatego sprawdzamy też obecność m.in. szkodliwych alkaloidów pirolizydynowych czy tlenku etylenu.
W naszych suplementach masz gwarancję, że ich nie znajdziesz!
Akredytowane laboratorium J. S. Hamilton Poland, w którym drugi raz sprawdzamy każdą partię suplementu

Z Science Care masz pewność, że otrzymasz suplement o czystym, przebadanym składzie wspierającym Twoje długotrwałe zdrowie i sprawność.



Co warto wiedzieć?

- Dwie kapsułki dziennie. Najlepiej przyjęte podczas jednego (idealnie pierwszego w danym dniu) posiłku i popite wodą.
- Mimo braku kofeiny, składniki pobudzają układ nerwowy i mają lekkie działanie stymulujące, więc ważne, aby przyjąć suplement w pierwszej połowie dnia.
- Nie należy przekraczać zalecanej porcji do spożycia w ciągu dnia (2 kapsułek).
- Przechowywać w temperaturze pokojowej.
- Chronić od światła i wilgoci.
- Przechowywać w sposób niedostępny dla małych dzieci.
- Suplement jest przeznaczony dla osób dorosłych po 18 roku życia.
- Nie stosować w przypadku nadwrażliwości na którykolwiek ze składników.
- Suplement nie jest przeznaczony dla dzieci, kobiet w ciąży oraz w trakcie laktacji.
- Dla utrzymania prawidłowego stanu zdrowia należy stosować zróżnicowaną dietę i prowadzić zdrowy tryb życia. Suplement diety nie może być stosowany jako substytut (zamiennik) zróżnicowanej diety.
Rozwojowiec Sp. z o. o. ul. Romana Dmowskiego 3/9, 50-203 Wrocław.

Wypróbuj BEZ RYZYKA dzięki 25-dniowej Bezwarunkowej Gwarancji Satysfakcji
Jeśli w trakcie przyjmowania suplementu z jakiegokolwiek powodu stwierdzisz, że nie jest dla Ciebie, możesz skorzystać z naszej 25-dniowej Bezwarunkowej Gwarancji Satysfakcji.
Wystarczy, że w ciągu 25 dni od dnia otrzymania swojego pierwszego zamówienia Science Care Pamięć i Koncentracja™ wypełnisz ten formularz i wyślesz go na adres: [email protected], a na adres: IMKER ul. Szczebrzeska 55, 22-400 Zamość prześlesz pozostałość niewykorzystanego produktu, a bez żadnych pytań zwrócimy Ci 100% ceny, którą za niego zapłaciłeś.
25 dni na zwrot

Oryginalny polski produkt


Naturalny przebadany skład
Zamówienia złożone od poniedziałku do piątku do godziny 11:00 wysyłamy tego samego dnia

Najczęściej zadawane pytania
Każdy organizm jest inny, więc efekty stosowania mogą być obserwowalne w nieco różnym czasie u różnych osób.
Jednak żeby dać jakiś punkt odniesienia: wg badań pewne poszczególne efekty (np. szybsze przetwarzanie informacji) mogą być widoczne już nawet kilka godzin po przyjęciu danego ekstraktu roślinnego.
Pierwsze efekty mogą się więc pojawić od razu — po pierwszej porcji lub pierwszych kilku dniach suplementacji.
Jednak większość analizowanych przez nas badań testowała okres suplementacji wynoszący 2-3 miesiące, więc są pewne przesłanki, że te 2-3 miesiące codziennej suplementacji to czas, po którym efekty stają się najbardziej widoczne.
Pisane 20.12.2022: Na tę chwilę wszyscy jeszcze bierzemy go krótko - od kilku dni, do max 2 tygodni (Damian), bo świeżo po tym jak go otrzymaliśmy, zaczęliśmy się przygotowywać do tego, żeby go Wam pokazać :). Ale tutaj jest garść naszych dotychczasowych wrażeń:
Paweł Niewiarczuk: ja mam wrażenie, że mam lepszą kontrolę emocji (mniej denerwuję się na psa np. na spacerach) i koncentrację (mniej się rozpraszam i potrafię być bardziej skupiony na zadaniu).
Plus zauważyłem u siebie na wynikach HRV w Garminie, że mam wzrost tego parametru od początku suplementacji.
Przypomnienie od Rozwojowca: wzrost HRV (zmienności rytmu zatokowego serca) oznacza wyższy poziom zregenerowania i ogólnej sprawności organizmu. Koreluje m.in. z większą zdolnością kontroli uwagi, emocji oraz większą sprawnością fizyczną.
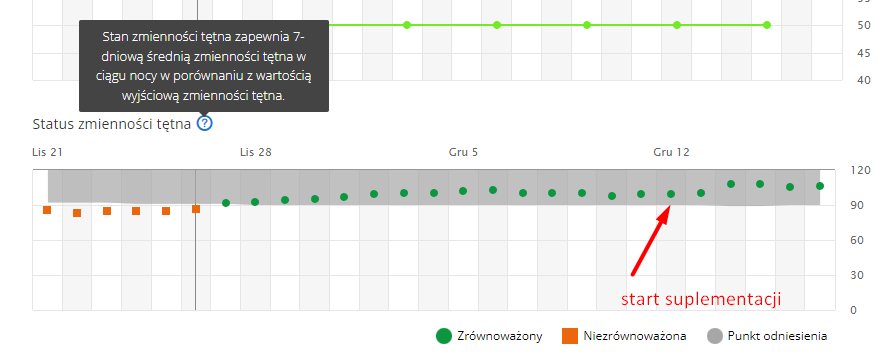
Damian Redmer: Ja biorę ok. 2 tygodnie.
Największą różnicę zauważyłem w większej odporności na stres. Raczej rzadko go doświadczam intensywnie, chyba że... mamy premierę czegoś nowego :) Tak jak teraz. Kilka dni przed premierą suplementu było okresem, w którym trzeba było dopinać MNÓSTWO rzeczy, a mi bardzo zależało, żeby wszystko poszło dobrze i się Wam spodobało :)
Stresujący i intensywny okres. Jak przed premierą czegokolwiek, co się tworzy.
Przy czym tym razem... ta cała intensywność jakby nie przedostawała się na poziom fizjologiczny. Myśli miałem te same co przy każdej premierze, obawy i nadzieje też, różne nieprzewidziane wydarzenia i opóźnienia też się pojawiły, ale to jakby nie przechodziło na poziom ciała. Nie było niepotrzebnego wyrzutu adrenaliny, nie czułem reakcji stresowej organizmu.
Mój oura ring potwierdził - załączam parametry z nocy przed dniem premiery (czyli najbardziej intensywny okres prac i stresu).
Wszystko w normie. Zero fizjologicznych objawów stresu. Sam byłem zdziwiony, że aż tak to u mnie zadziałało.
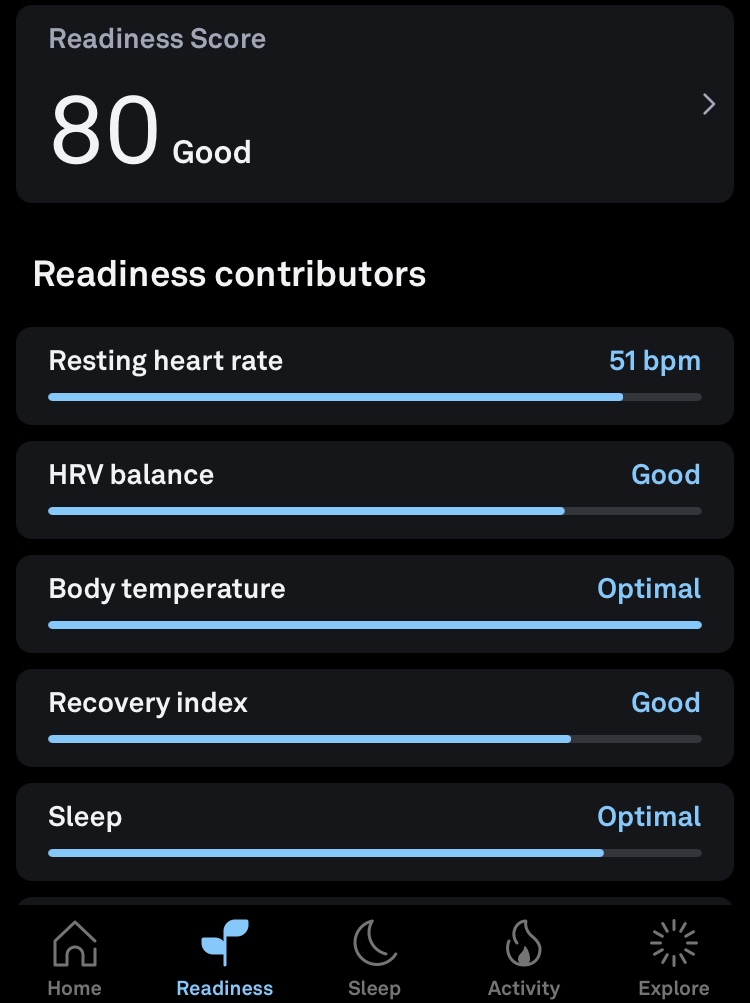
Adam M. Obara: Ja zażywam krótko (niewiele ponad tydzień). Łatwiej mi utrzymywać uwagę w czasie treningu koncentracji (myśli przychodzą jak zwykle, ale o wiele szybciej je zwalczam, nie zdarza mi się już tak często zapominać, przy której jestem liczbie, rzadziej rozmywa mi się wizualizacja).
Dodatkowe, co zauważyłem, to zwiększenie prędkości reakcji (jak mam kilka minut gram w gry, w których timing jest ważny - rytmiczne itd. Jestem ogólnie na dość wysokim poziomie, ale od dłuższego czasu byłem na raczej stałym poziomie; w ciągu ostatnich 2-3 dni pobiłem większość swoich dotychczasowych najlepszych wyników.
Klaudia Blicharska: U siebie zauważyłam pierwsze efekty już w drugim dniu stosowania, na początku nawet do głowy mi nie przyszło, że to może już być spowodowane suplementem.
Ogólnie czułam lepsze samopoczucie, większy hmmm luz w ciele, a przede wszystkim, gdy z kimś rozmawiałam lub siadałam do odpisywania na maile, zauważyłam, że jakoś szybciej kojarzę fakty - po prostu lepiej i szybciej myślałam. Jak pojawiały się jakieś myśli, które zaczynały mnie sabotować, to zaraz nagle przypominały mi się różne techniki, narzędzia, ogólnie wiedza związana z tym konkretnym wątkiem, którą kiedyś poznałam i mogę jej użyć.
Z dwóch źródeł — z badań i praktyki.
Badania — żadne naukowe źródła nie znalazły negatywnych interakcji pomiędzy składnikami suplementu.
Praktyka — to nie jest tak, że my jako pierwsi odkryliśmy te rośliny — od lat na rynku są setki innych suplementów, które zawierają w sobie praktycznie każdą kombinację składników z naszego.
Nasz własny suplement stworzyliśmy nie dlatego, że nie da się dostać suplementów, które zawierają ekstrakty z roślin, które znaleźliśmy (bo się da), tylko dlatego, że:
- Chcieliśmy, aby w suplemencie były TYLKO te ekstrakty. Żadnej kofeiny, żadnych innych substancji właśnie po to, aby dało się bezpiecznie łączyć ten suplement z innymi.
- Chcieliśmy, aby ekstrakty były w takich stężeniach i takich ilościach, które wg badań dają efekty i są bezpieczne. O ile prosto (niekoniecznie opłacalnie) da się kupić i brać każdy składnik suplementu osobno, o tyle naprawdę trudno w ten sposób brać ich odpowiednią ilość. Często będzie wtedy zbyt dużo jednego składnika, zbyt mało innego, a porcja tutaj jest kluczowa.
- Chcieliśmy mieć pewność, że w naszym suplemencie nie będzie żadnych szkodliwych dodatków (tlenek etylenu, alkaloidy, metale ciężkie itp.). W chwili pisania tych słów nie widzieliśmy żadnego suplementu, który informowałby na stronie, że jest przebadany tak szeroko, jak nasz.
Podsumowując — interakcje między składnikami już dawno sprawdzili inni, bo suplementy ze zbliżonym składem istnieją od lat. Nie dla kombinacji tych składników stworzyliśmy własny suplement (bo przecież mogliśmy sobie kupić osobno składniki i je brać). Tylko głównie dla odpowiednich porcji i stężeń każdego ekstraktu oraz pewności, że w środku nie ma niczego szkodliwego, aby móc brać ten suplement codziennie latami.
Ze względu na brak wystarczających badań na tych grupach.
Po prostu brakuje informacji, bo stosunkowo rzadko prowadzi się badania związane z suplementacją na osobach poniżej 18 roku życia oraz na kobietach w ciąży czy laktacji. To zresztą nie dotyczy tylko suplementacji, ale tez wielu innych substancji, leków czy interwencji np. w fizykoterapii.
Stąd te standardowe zalecenia bezpieczeństwa.
Niestety na tę chwilę realizujemy zamówienia tylko na terenie Polski. Jednak w związku z licznymi zapytaniami badamy opcje wprowadzenia wysyłek zagranicznych.
Jeśli jesteś zainteresowany suplementem, ale mieszkasz za granicą, to napisz do nas na [email protected] z informacją, w jakim kraju obecnie mieszkasz. Jeśli wprowadzimy wysyłkę zagraniczną do tego kraju, to damy Ci emailowo o tym znać.
Nie wiadomo czy większa ilość da długotrwale większe efekty. W biologii nie ma zasady, że “więcej znaczy lepiej”. W suplemencie każdy ekstrakt został użyty w takiej porcji i koncentracji, co do której zmierzono, iż daje wyraźne korzyści.
Eksperymentując z większymi porcjami, nie ma gwarancji, że osiągnie się jeszcze większe efekty, plus dochodzi wtedy pytanie o wpływ takich dawek na długotrwałe zdrowie czy np. na wątrobę.
To zawsze dawka czyni truciznę. W zbyt dużej ilości dosłownie wszystko jest szkodliwe - dowolny produkt spożywczy, witaminy, nawet woda (to tzw. przewodnienie izotoniczne i grozi np. maratończykom). Każda z tych roślin więc z pewnością także.
Dlatego poza tym, że dobraliśmy takie parametry każdego ekstraktu, co do których jest naukowa pewność, że działają, to zastosowaliśmy się także do maksymalnych norm prawnych, bo one mają na celu właśnie utrzymanie długotrwałego zdrowia i bazują m.in. na opiniach EFSA (Europejskiego Urzędu ds. Bezpieczeństwa Żywności) i także na badaniach dotyczących bezpiecznej suplementacji tych roślin.
Więc podsumowując:
- Czy można osiągnąć długotrwale większe korzyści przekraczając dzienną dawkę suplementu lub biorąc dodatkowo jeszcze więcej któregoś z jego ekstraktów? Nie ma pewności.
- Czy takie przekroczenie norm jest długotrwale korzystne dla ogólnego zdrowia? Prawdopodobnie nie.
- Czy każdy ekstrakt w suplemencie jest w takiej ilości, aby dawał efekty i jednocześnie jego długotrwałe stosowanie było bezpieczne? Tak.
Nie ma ku temu jasnych przeciwwskazań, choć kofeina może potęgować pobudzający efekt suplementu m.in. ze względu na zawartość żeń-szenia koreańskiego.
Dlatego są też na rynku dostępne suplementy diety zawierające ekstrakty roślinne obecne w Science Care Pamięć i Koncentracja, które dodatkowo zawierają w składzie kofeinę.
Przy czym należy pamiętać, aby nie popijać suplementu kawą czy herbatą, gdyż zawierają one dużo garbników, które mogą ograniczać wchłanianie składników aktywnych z suplementu.
Najlepiej popić go więc czystą wodą i zachować przynajmniej 1 godzinę odstępu między suplementacją, a np. filiżanką kawy.
Obecnie nie ma badań świadczących o tym, że przyjmowanie ekstraktów użytych w Science Care Pamięć i Koncentracja przez dłuższy czas jest w jakikolwiek sposób szkodliwe dla zdrowia. Przeciwnie — dobraliśmy takie ekstrakty i w takich ilościach, aby to zdrowie wspierały.
Przykładowo istnieją badania, które sprawdzały m.in. efekty codziennego przyjmowania ashwagandhy i bakopy drobnolistnej przez rok i nie stwierdziły żadnych efektów ubocznych.
Przy czym jest bardzo mało badań sprawdzających skutki ciągłej suplementacji powyżej roku — nie tylko ekstraktów roślinnych, ale praktycznie czegokolwiek.
Z tego względu generalną zalecaną praktyką (którą też polecamy w przypadku Science Care Pamięć i Koncentracja) jest wykonanie 1 miesiąca przerwy w suplementacji po każdych 3 miesiącach codziennego stosowania.
Obsługujemy wszystkie najpopularniejsze metody płatności takie jak płatność przelewem online, przelewem tradycyjnym, Płatność przez PayPal, płatność blikiem lub kartą.
Po wybraniu pakietu zostaniesz przekierowany na stronę z danymi do wysyłki (na niej możesz też wpisać dane do faktury, gdybyś potrzebował). Gdy ją uzupełnisz, zostaniesz przekierowany na stronę Przelewy24, gdzie będziesz mógł wybrać formę płatności.
Jedynie opcja płatności kartą jest bardziej “schowana”. Aby nią zapłacić na stronie Przelewy24 w menu po lewej kliknij “Inne” i wybierz opcję z symbolem PayPal. Ta forma płatności pozwala zapłacić kartą, nawet jeśli nie masz konta na PayPalu.
Zamówienia złożone do godziny 11:00 w dni robocze realizowane są jeszcze tego samego dnia.
Sama paczka zostanie doręczona za pośrednictwem firmy kurierskiej, poczty lub do wybranego paczkomatu. Pełen koszt przesyłki poznasz podczas składania zamówienia, wybierając pakiet 3 lub 6 opakowań, koszty przesyłki na terenie kraju pokrywamy my.
Dzienna dawka Science Care Pamięć i Koncentracja™ to dwie kapsułki przyjęte na raz podczas posiłku i popite wodą. Suplement ma działanie stymulujące, więc nie zaleca się przyjmowanie go na kilka godzin przed snem.
Nie należy przekraczać zalecanej porcji do spożycia w ciągu dnia (2 kapsułek).
Ze względu na potencjalne interakcje przyjmowanie Science Care Pamięć i Koncentracja™ wraz z lekami najlepiej skonsultować z lekarzem lub farmaceutą.
Produkt zawiera w składzie ashwagandhę, dlatego nie powinien być on spożywany w przypadku stosowania leków o działaniu uspokajającym, nasennym oraz przeciwpadaczkowym.
Termin przydatności do spożycia wynosi 2 lata od daty produkcji.
Termin, przed którym należy spożyć suplement, jest podany na etykiecie każdego suplementu.
Kontakt
Jeśli masz pytania związane
z suplementem Science Care Pamięć
i Koncentracja™ – napisz, postaramy się pomóc.
Klikając wyślij wyrażasz zgodę na przetwarzanie Twoich danych osobowych w celu odpowiedzi na Twoją wiadomość mailową i na zasadach określonych w polityce prywatności. Podane dane mogą być wykorzystywane w celach marketingowych, jeśli będzie wymagała tego odpowiedź. Administratorem danych osobowych jest Rozwojowiec Sp. z o.o. z siedzibą przy ul. Romana Dmowskiego 3/9, 50-203 Wrocław, KRS 0000943812.
Bibliografia
W bazie naukowej PubMed istnieje ponad 17036 publikacji naukowych dotyczących składników, które znalazły się w składzie Science Care Pamięć i Koncentracja™. W poniższej bibliografii wybrano te z nich, które popierają ich działanie w obszarach wymienionych w sekcji „Skład i działanie poparte badaniami naukowymi”.
Ashwagandha
- Choudhary, D., Bhattacharyya, S., & Bose, S. (2017). Efficacy and Safety of Ashwagandha (Withania somnifera (L.) Dunal) Root Extract in Improving Memory and Cognitive Functions. Journal of dietary supplements, 14(6), 599–612. doi:10.1080/19390211.2017.1284970
- Gopukumar, K., Thanawala, S., Somepalli, V., Rao, T., Thamatam, V. B., & Chauhan, S. (2021). Efficacy and Safety of Ashwagandha Root Extract on Cognitive Functions in Healthy, Stressed Adults: A Randomized, Double-Blind, Placebo-Controlled Study. Evidence-based complementary and alternative medicine : eCAM, 2021, 8254344. doi:10.1155/2021/8254344
- Ng, Q. X., Loke, W., Foo, N. X., Tan, W. J., Chan, H. W., Lim, D. Y., & Yeo, W. S. (2020). A systematic review of the clinical use of Withania somnifera (Ashwagandha) to ameliorate cognitive dysfunction. Phytotherapy research : PTR, 34(3), 583–590. doi:10.1002/ptr.6552
- Remenapp, A., Coyle, K., Orange, T., Lynch, T., Hooper, D., Hooper, S., Conway, K., & Hausenblas, H. A. (2021). Efficacy of Withania somnifera supplementation on adult's cognition and mood. Journal of Ayurveda and integrative medicine, 13(2), 100510. Advance online publication. doi:10.1016/j.jaim.2021.08.003
- Chengappa, K. N., Bowie, C. R., Schlicht, P. J., Fleet, D., Brar, J. S., & Jindal, R. (2013). Randomized placebo-controlled adjunctive study of an extract of withania somnifera for cognitive dysfunction in bipolar disorder. The Journal of clinical psychiatry, 74(11), 1076–1083. doi:10.4088/JCP.13m08413
- Dimpfel, W., Schombert, L., Keplinger-Dimpfel, I. K., & Panossian, A. (2020). Effects of an Adaptogenic Extract on Electrical Activity of the Brain in Elderly Subjects with Mild Cognitive Impairment: A Randomized, Double-Blind, Placebo-Controlled, Two-Armed Cross-Over Study. Pharmaceuticals (Basel, Switzerland), 13(3), 45. doi:10.3390/ph13030045
- Naidu, P. S., Singh, A., & Kulkarni, S. K. (2006). Effect of Withania somnifera root extract on reserpine-induced orofacial dyskinesia and cognitive dysfunction. Phytotherapy research : PTR, 20(2), 140–146. doi:10.1002/ptr.1823
- Zhao, J., Nakamura, N., Hattori, M., Kuboyama, T., Tohda, C., & Komatsu, K. (2002). Withanolide derivatives from the roots of Withania somnifera and their neurite outgrowth activities. Chemical & pharmaceutical bulletin, 50(6), 760–765
- Tohda C, Joyashiki E. Sominone enhances neurite outgrowth and spatial memory mediated by the neurotrophic factor receptor, RET. Br J Pharmacol. 2009 Aug;157(8):1427-40. doi: 10.1111/j.1476-5381.2009.00313.x.
- Pingali, U., Pilli, R., & Fatima, N. (2014). Effect of standardized aqueous extract of Withania somnifera on tests of cognitive and psychomotor performance in healthy human participants. Pharmacognosy research, 6(1), 12–18. doi:10.4103/0974-8490.122912
- Soman, S., Korah, P. K., Jayanarayanan, S., Mathew, J., & Paulose, C. S. (2012). Oxidative stress induced NMDA receptor alteration leads to spatial memory deficits in temporal lobe epilepsy: ameliorative effects of Withania somnifera and Withanolide A. Neurochemical research, 37(9), 1915–1927. doi:10.1007/s11064-012-0810-5
- Rege, N. N., Thatte, U. M., & Dahanukar, S. A. (1999). Adaptogenic properties of six rasayana herbs used in Ayurvedic medicine. Phytotherapy research : PTR, 13(4), 275–291. doi: 10.1002/(SICI)1099-1573(199906)13:4<275::AID-PTR510>3.0.CO;2-S
- Singh, B., Chandan, B. K., & Gupta, D. K. (2003). Adaptogenic activity of a novel withanolide-free aqueous fraction from the roots of Withania somnifera Dun. (Part II). Phytotherapy research : PTR, 17(5), 531–536. doi: 10.1002/ptr.1189
- Salve, J., Pate, S., Debnath, K., & Langade, D. (2019). Adaptogenic and Anxiolytic Effects of Ashwagandha Root Extract in Healthy Adults: A Double-blind, Randomized, Placebo-controlled Clinical Study. Cureus, 11(12), e6466. doi:10.7759/cureus.6466
- Panossian, A., & Wikman, G. (2010). Effects of Adaptogens on the Central Nervous System and the Molecular Mechanisms Associated with Their Stress-Protective Activity. Pharmaceuticals (Basel, Switzerland), 3(1), 188–224. https://doi.org/10.3390/ph3010188
- Biswal, B. M., Sulaiman, S. A., Ismail, H. C., Zakaria, H., & Musa, K. I. (2013). Effect of Withania somnifera (Ashwagandha) on the development of chemotherapy-induced fatigue and quality of life in breast cancer patients. Integrative cancer therapies, 12(4), 312–322. doi: 10.1177/1534735412464551
- Bonilla, D. A., Moreno, Y., Gho, C., Petro, J. L., Odriozola-Martínez, A., & Kreider, R. B. (2021). Effects of Ashwagandha (Withania somnifera) on Physical Performance: Systematic Review and Bayesian Meta-Analysis. Journal of functional morphology and kinesiology, 6(1), 20. doi:10.3390/jfmk6010020
- Pérez-Gómez, J., Villafaina, S., Adsuar, J. C., Merellano-Navarro, E., & Collado-Mateo, D. (2020). Effects of Ashwagandha (Withania somnifera) on VO2max: A Systematic Review and Meta-Analysis. Nutrients, 12(4), 1119. doi:10.3390/nu12041119
- Speers, A. B., Cabey, K. A., Soumyanath, A., & Wright, K. M. (2021). Effects of Withania somnifera (Ashwagandha) on Stress and the Stress- Related Neuropsychiatric Disorders Anxiety, Depression, and Insomnia. Current neuropharmacology, 19(9), 1468–1495. doi: 10.2174/1570159X19666210712151556
- Lopresti, A. L., Smith, S. J., Malvi, H., & Kodgule, R. (2019). An investigation into the stress-relieving and pharmacological actions of an ashwagandha (Withania somnifera) extract: A randomized, double-blind, placebo-controlled study. Medicine, 98(37), e17186. doi: 10.1097/MD.0000000000017186
- Chandrasekhar, K., Kapoor, J., & Anishetty, S. (2012). A prospective, randomized double-blind, placebo-controlled study of safety and efficacy of a high-concentration full-spectrum extract of ashwagandha root in reducing stress and anxiety in adults. Indian journal of psychological medicine, 34(3), 255–262. doi:10.4103/0253-7176.106022
- Mishra, L. C., Singh, B. B., & Dagenais, S. (2000). Scientific basis for the therapeutic use of Withania somnifera (ashwagandha): a review. Alternative medicine review : a journal of clinical therapeutic, 5(4), 334–346.
- Langade, D., Kanchi, S., Salve, J., Debnath, K., & Ambegaokar, D. (2019). Efficacy and Safety of Ashwagandha (Withania somnifera) Root Extract in Insomnia and Anxiety: A Double-blind, Randomized, Placebo-controlled Study. Cureus, 11(9), e5797. doi: 0.7759/cureus.5797
- Cheah, K. L., Norhayati, M. N., Husniati Yaacob, L., & Abdul Rahman, R. (2021). Effect of Ashwagandha (Withania somnifera) extract on sleep: A systematic review and meta-analysis. PloS one, 16(9), e0257843. doi:10.1371/journal.pone.0257843
- Langade, D., Thakare, V., Kanchi, S., & Kelgane, S. (2021). Clinical evaluation of the pharmacological impact of ashwagandha root extract on sleep in healthy volunteers and insomnia patients: A double-blind, randomized, parallel-group, placebo-controlled study. Journal of ethnopharmacology, 264, 113276. doi: 10.1016/j.jep.2020.113276
- Deshpande, A., Irani, N., Balkrishnan, R., & Benny, I. R. (2020). A randomized, double blind, placebo controlled study to evaluate the effects of ashwagandha (Withania somnifera) extract on sleep quality in healthy adults. Sleep medicine, 72, 28–36. doi: 10.1016/j.sleep.2020.03.012
- Cheah, K. L., Norhayati, M. N., Husniati Yaacob, L., & Abdul Rahman, R. (2021). Effect of Ashwagandha (Withania somnifera) extract on sleep: A systematic review and meta-analysis. PloS one, 16(9), e0257843. doi: 10.1371/journal.pone.0257843
- Kelgane, S. B., Salve, J., Sampara, P., & Debnath, K. (2020). Efficacy and Tolerability of Ashwagandha Root Extract in the Elderly for Improvement of General Well-being and Sleep: A Prospective, Randomized, Double-blind, Placebo-controlled Study. Cureus, 12(2), e7083. doi: 10.7759/cureus.7083
- Raut, A. A., Rege, N. N., Tadvi, F. M., Solanki, P. V., Kene, K. R., Shirolkar, S. G., Pandey, S. N., Vaidya, R. A., & Vaidya, A. B. (2012). Exploratory study to evaluate tolerability, safety, and activity of Ashwagandha (Withania somnifera) in healthy volunteers. Journal of Ayurveda and integrative medicine, 3(3), 111–114. doi: 10.4103/0975-9476.100168
- Pratte, M. A., Nanavati, K. B., Young, V., & Morley, C. P. (2014). An alternative treatment for anxiety: a systematic review of human trial results reported for the Ayurvedic herb ashwagandha (Withania somnifera). Journal of alternative and complementary medicine (New York, N.Y.), 20(12), 901–908. doi:10.1089/acm.2014.0177
- Sarris, J. (2018). Herbal medicines in the treatment of psychiatric disorders: 10-year updated review. Phytotherapy Research, 32(7), 1147–1162. doi:10.1002/ptr.6055
- Wankhede, S., Langade, D., Joshi, K., Sinha, S. R., & Bhattacharyya, S. (2015). Examining the effect of Withania somnifera supplementation on muscle strength and recovery: a randomized controlled trial. Journal of the International Society of Sports Nutrition, 12, 43. doi: 10.1186/s12970-015-0104-9
- Dongre, S., Langade, D., & Bhattacharyya, S. (2015). Efficacy and Safety of Ashwagandha (Withania somnifera) Root Extract in Improving Sexual Function in Women: A Pilot Study. BioMed research international, 2015, 284154. doi: 10.1155/2015/284154
- Ambiye, V. R., Langade, D., Dongre, S., Aptikar, P., Kulkarni, M., & Dongre, A. (2013). Clinical Evaluation of the Spermatogenic Activity of the Root Extract of Ashwagandha (Withania somnifera) in Oligospermic Males: A Pilot Study. Evidence-based complementary and alternative medicine : eCAM, 2013, 571420. doi: 10.1155/2013/571420
- Singh, N., Bhalla, M., de Jager, P., & Gilca, M. (2011). An overview on ashwagandha: a Rasayana (rejuvenator) of Ayurveda. African journal of traditional, complementary, and alternative medicines : AJTCAM, 8(5 Suppl), 208–213. doi: 10.4314/ajtcam.v8i5S.9
- Tiwari, S., Gupta, S. K., & Pathak, A. K. (2021). A double-blind, randomized, placebo-controlled trial on the effect of Ashwagandha (Withania somnifera dunal.) root extract in improving cardiorespiratory endurance and recovery in healthy athletic adults. Journal of ethnopharmacology, 272, 113929. doi: 10.1016/j.jep.2021.113929
Panax ginseng i Panax quinquefolius L. - Lee, S. T., Chu, K., Sim, J. Y., Heo, J. H., & Kim, M. (2008). Panax ginseng enhances cognitive performance in Alzheimer disease. Alzheimer disease and associated disorders, 22(3), 222–226. doi: 10.1097/WAD.0b013e31816c92e6
- Lee, Y., & Oh, S. (2015). Administration of red ginseng ameliorates memory decline in aged mice. Journal of ginseng research, 39(3), 250–256. doi: 10.1016/j.jgr.2015.01.003
- Kennedy D. O. (2019). Phytochemicals for Improving Aspects of Cognitive Function and Psychological State Potentially Relevant to Sports Performance. Sports medicine (Auckland, N.Z.), 49(Suppl 1), 39–58. doi: 10.1007/s40279-018-1007-0
- Wesnes, K. A., Ward, T., McGinty, A., & Petrini, O. (2000). The memory enhancing effects of a Ginkgo biloba/Panax ginseng combination in healthy middle-aged volunteers. Psychopharmacology, 152(4), 353–361. doi: 10.1007/s002130000533
- Mariage, P. A., Hovhannisyan, A., & Panossian, A. G. (2020). Efficacy of Panax ginseng Meyer Herbal Preparation HRG80 in Preventing and Mitigating Stress-Induced Failure of Cognitive Functions in Healthy Subjects: A Pilot, Randomized, Double-Blind, Placebo-Controlled Crossover Trial. Pharmaceuticals (Basel, Switzerland), 13(4), 57. doi: 10.3390/ph13040057
- Ju, S., Seo, J. Y., Lee, S. K., Oh, J., & Kim, J. S. (2021). Oral administration of hydrolyzed red ginseng extract improves learning and memory capability of scopolamine-treated C57BL/6J mice via upregulation of Nrf2-mediated antioxidant mechanism. Journal of ginseng research, 45(1), 108–118. doi: 10.1016/j.jgr.2019.12.005
- Chen, C., Zhang, H., Xu, H., Zheng, Y., Wu, T., & Lian, Y. (2019). Ginsenoside Rb1 ameliorates cisplatin-induced learning and memory impairments. Journal of ginseng research, 43(4), 499–507. doi: 10.1016/j.jgr.2017.07.009
- Liu, L., Hoang-Gia, T., Wu, H., Lee, M. R., Gu, L., Wang, C., Yun, B. S., Wang, Q., Ye, S., & Sung, C. K. (2011). Ginsenoside Rb1 improves spatial learning and memory by regulation of cell genesis in the hippocampal subregions of rats. Brain research, 1382, 147–154. doi: 10.1016/j.brainres.2011.01.051
- Reay, J. L., Kennedy, D. O., & Scholey, A. B. (2005). Single doses of Panax ginseng (G115) reduce blood glucose levels and improve cognitive performance during sustained mental activity. Journal of psychopharmacology (Oxford, England), 19(4), 357–365. doi: 10.1177/0269881105053286
- Zhu, J. D., Wang, J. J., Zhang, X. H., Yu, Y., & Kang, Z. S. (2018). Panax ginseng extract attenuates neuronal injury and cognitive deficits in rats with vascular dementia induced by chronic cerebral hypoperfusion. Neural regeneration research, 13(4), 664–672. doi: 10.4103/1673-5374.230292
- Park, K. C., Jin, H., Zheng, R., Kim, S., Lee, S. E., Kim, B. H., & Yim, S. V. (2019). Cognition enhancing effect of panax ginseng in Korean volunteers with mild cognitive impairment: a randomized, double-blind, placebo-controlled clinical trial. Translational and clinical pharmacology, 27(3), 92–97. doi: 10.12793/tcp.2019.27.3.92
- Reay, J. L., Kennedy, D. O., & Scholey, A. B. (2006). Effects of Panax ginseng, consumed with and without glucose, on blood glucose levels and cognitive performance during sustained 'mentally demanding' tasks. Journal of psychopharmacology (Oxford, England), 20(6), 771–781. doi: 10.1177/0269881106061516
- Arring, N. M., Millstine, D., Marks, L. A., & Nail, L. M. (2018). Ginseng as a Treatment for Fatigue: A Systematic Review. Journal of alternative and complementary medicine (New York, N.Y.), 24(7), 624–633. doi: 10.1089/acm.2017.0361
- Lu, G., Liu, Z., Wang, X., & Wang, C. (2021). Recent Advances in Panax ginseng C.A. Meyer as a Herb for Anti-Fatigue: An Effects and Mechanisms Review. Foods (Basel, Switzerland), 10(5), 1030. doi: 10.3390/foods10051030
- Jin, T. Y., Rong, P. Q., Liang, H. Y., Zhang, P. P., Zheng, G. Q., & Lin, Y. (2020). Clinical and Preclinical Systematic Review of Panax ginseng C. A. Mey and Its Compounds for Fatigue. Frontiers in pharmacology, 11, 1031. doi: 10.3389/fphar.2020.01031
- Irfan, M., Kwak, Y. S., Han, C. K., Hyun, S. H., & Rhee, M. H. (2020). Adaptogenic effects of Panax ginseng on modulation of cardiovascular functions. Journal of ginseng research, 44(4), 538–543. doi: 10.1016/j.jgr.2020.03.001
- Kim J. H. (2018). Pharmacological and medical applications of Panax ginseng and ginsenosides: a review for use in cardiovascular diseases. Journal of ginseng research, 42(3), 264–269. doi: 10.1016/j.jgr.2017.10.004
- Hyun, S. H., Bhilare, K. D., In, G., Park, C. K., & Kim, J. H. (2022). Effects of Panax ginseng and ginsenosides on oxidative stress and cardiovascular diseases: pharmacological and therapeutic roles. Journal of ginseng research, 46(1), 33–38. doi: 10.1016/j.jgr.2021.07.007
- Tian, J., Fu, F., Geng, M., Jiang, Y., Yang, J., Jiang, W., Wang, C., & Liu, K. (2005). Neuroprotective effect of 20(S)-ginsenoside Rg3 on cerebral ischemia in rats. Neuroscience letters, 374(2), 92–97. doi: 10.1016/j.neulet.2004.10.030
- Zhou, P., Xie, W., Sun, Y., Dai, Z., Li, G., Sun, G., & Sun, X. (2019). Ginsenoside Rb1 and mitochondria: A short review of the literature. Molecular and cellular probes, 43, 1–5. doi: 10.1016/j.mcp.2018.12.001
- Sharma, A., & Lee, H. J. (2020). Ginsenoside Compound K: Insights into Recent Studies on Pharmacokinetics and Health-Promoting Activities. Biomolecules, 10(7), 1028. doi: 10.3390/biom10071028
- Shergis, J. L., Zhang, A. L., Zhou, W., & Xue, C. C. (2013). Panax ginseng in randomised controlled trials: a systematic review. Phytotherapy research : PTR, 27(7), 949–965. soi: 10.1002/ptr.4832
- He, L. X., Ren, J. W., Liu, R., Chen, Q. H., Zhao, J., Wu, X., Zhang, Z. F., Wang, J. B., Pettinato, G., & Li, Y. (2017). Ginseng (Panax ginseng Meyer) oligopeptides regulate innate and adaptive immune responses in mice via increased macrophage phagocytosis capacity, NK cell activity and Th cells secretion. Food & function, 8(10), 3523–3532. doi: 10.1039/c7fo00957g
- Ratan, Z. A., Youn, S. H., Kwak, Y. S., Han, C. K., Haidere, M. F., Kim, J. K., Min, H., Jung, Y. J., Hosseinzadeh, H., Hyun, S. H., & Cho, J. Y. (2021). Adaptogenic effects of Panax ginseng on modulation of immune functions. Journal of ginseng research, 45(1), 32–40. doi: 10.1016/j.jgr.2020.09.004
- Liu, J., Nile, S. H., Xu, G., Wang, Y., & Kai, G. (2021). Systematic exploration of Astragalus membranaceus and Panax ginseng as immune regulators: Insights from the comparative biological and computational analysis. Phytomedicine : international journal of phytotherapy and phytopharmacology, 86, 153077. doi: 10.1016/j.phymed.2019.153077
- Scaglione, F., Cattaneo, G., Alessandria, M., & Cogo, R. (1996). Efficacy and safety of the standardised Ginseng extract G115 for potentiating vaccination against the influenza syndrome and protection against the common cold [corrected]. Drugs under experimental and clinical research, 22(2), 65–72.
- Na, H. S., Lim, Y. J., Yun, Y. S., Kweon, M. N., & Lee, H. C. (2010). Ginsan enhances humoral antibody response to orally delivered antigen. Immune network, 10(1), 5–14. doi: 10.4110/in.2010.10.1.5
- Seo, J. Y., Choi, J. W., Lee, J. Y., Park, Y. S., & Park, Y. I. (2018). Enzyme Hydrolysates of Ginseng Marc Polysaccharides Promote the Phagocytic Activity of Macrophages Via Activation of TLR2 and Mer Tyrosine Kinase. Journal of microbiology and biotechnology, 28(6), 860–873. doi: 10.4014/jmb.1801.01003
- Panossian, A., & Brendler, T. (2020). The Role of Adaptogens in Prophylaxis and Treatment of Viral Respiratory Infections. Pharmaceuticals (Basel, Switzerland), 13(9), 236. doi: 10.3390/ph13090236
- Dang, H., Chen, Y., Liu, X., Wang, Q., Wang, L., Jia, W., & Wang, Y. (2009). Antidepressant effects of ginseng total saponins in the forced swimming test and chronic mild stress models of depression. Progress in neuro-psychopharmacology & biological psychiatry, 33(8), 1417–1424. doi: 10.1016/j.pnpbp.2009.07.020
- Jiang, R., Wang, M., Shi, L., Zhou, J., Ma, R., Feng, K., Chen, X., Xu, X., Li, X., Li, T., & Sun, L. (2019). Panax ginseng Total Protein Facilitates Recovery from Dexamethasone-Induced Muscle Atrophy through the Activation of Glucose Consumption in C2C12 Myotubes. BioMed research international, 2019, 3719643. doi: 10.1155/2019/3719643
- Cristina-Souza, G., Santos-Mariano, A. C., Lima-Silva, A. E., Costa, P. L., Domingos, P. R., Silva, S. F., Abreu, W. C., De-Oliveira, F. R., & Osiecki, R. (2022). Panax ginseng Supplementation Increases Muscle Recruitment, Attenuates Perceived Effort, and Accelerates Muscle Force Recovery After an Eccentric-Based Exercise in Athletes. Journal of strength and conditioning research, 36(4), 991–997. doi: 10.1519/JSC.0000000000003555
- Jung, H. L., Kwak, H. E., Kim, S. S., Kim, Y. C., Lee, C. D., Byurn, H. K., & Kang, H. Y. (2011). Effects of Panax ginseng supplementation on muscle damage and inflammation after uphill treadmill running in humans. The American journal of Chinese medicine, 39(3), 441–450. doi: 10.1142/S0192415X11008944
- Bang, V., Aranão, A., Nogueira, B. Z., Araújo, A. C., Bueno, P., Barbalho, S. M., de Souza, M., & Guiguer, E. L. (2019). Effects of Rhodiola rosea and Panax ginseng on the Metabolic Parameters of Rats Submitted to Swimming. Journal of medicinal food, 22(10), 1087–1090. doi: 10.1089/jmf.2019.0062
- Bao, L., Cai, X., Wang, J., Zhang, Y., Sun, B., & Li, Y. (2016). Anti-Fatigue Effects of Small Molecule Oligopeptides Isolated from Panax ginseng C. A. Meyer in Mice. Nutrients, 8(12), 807. doi: 10.3390/nu8120807
- Wang, J., Li, S., Fan, Y., Chen, Y., Liu, D., Cheng, H., Gao, X., & Zhou, Y. (2010). Anti-fatigue activity of the water-soluble polysaccharides isolated from Panax ginseng C. A. Meyer. Journal of ethnopharmacology, 130(2), 421–423. doi: 10.1016/j.jep.2010.05.027
- Bucci L. R. (2000). Selected herbals and human exercise performance. The American journal of clinical nutrition, 72(2 Suppl), 624S–36S. doi: 10.1093/ajcn/72.2.624S
- Abdelazim, A., Khater, S., Ali, H., Shalaby, S., Afifi, M., Saddick, S., Alkaladi, A., & Almaghrabi, O. A. (2019). Panax ginseng improves glucose metabolism in streptozotocin-induced diabetic rats through 5' adenosine monophosphate kinase up-regulation. Saudi journal of biological sciences, 26(7), 1436–1441. doi: 10.1016/j.sjbs.2018.06.001
- Park, M. W., Ha, J., & Chung, S. H. (2008). 20(S)-ginsenoside Rg3 enhances glucose-stimulated insulin secretion and activates AMPK. Biological & pharmaceutical bulletin, 31(4), 748–751. doi: 10.1248/bpb.31.748
- Pyke R. E. (2020). Sexual Performance Anxiety. Sexual medicine reviews, 8(2), 183–190. doi: 10.1016/j.sxmr.2019.07.001
- Brunetti, P., Lo Faro, A. F., Tini, A., Busardò, F. P., & Carlier, J. (2020). Pharmacology of Herbal Sexual Enhancers: A Review of Psychiatric and Neurological Adverse Effects. Pharmaceuticals, 13(10), 309. doi:10.3390/ph13100309
- Lee, H. W., Lee, M. S., Kim, T. H., Alraek, T., Zaslawski, C., Kim, J. W., & Moon, D. G. (2021). Ginseng for erectile dysfunction. The Cochrane database of systematic reviews, 4(4), CD012654. doi: 10.1002/14651858.CD012654.pub2
- Ghorbani, Z., Mirghafourvand, M., Charandabi, S. M., & Javadzadeh, Y. (2019). The effect of ginseng on sexual dysfunction in menopausal women: A double-blind, randomized, controlled trial. Complementary therapies in medicine, 45, 57–64. doi: 10.1016/j.ctim.2019.05.015
- Szczuka, D., Nowak, A., Zakłos-Szyda, M., Kochan, E., Szymańska, G., Motyl, I., & Blasiak, J. (2019). American Ginseng (Panax quinquefolium L.) as a Source of Bioactive Phytochemicals with Pro-Health Properties. Nutrients, 11(5), 1041. doi: 10.3390/nu11051041
- Arring, N. M., Millstine, D., Marks, L. A., & Nail, L. M. (2018). Ginseng as a Treatment for Fatigue: A Systematic Review. Journal of alternative and complementary medicine (New York, N.Y.), 24(7), 624–633. doi:10.1089/acm.2017.0361
- Barton, D. L., Liu, H., Dakhil, S. R., Linquist, B., Sloan, J. A., Nichols, C. R., McGinn, T. W., Stella, P. J., Seeger, G. R., Sood, A., & Loprinzi, C. L. (2013). Wisconsin Ginseng (Panax quinquefolius) to improve cancer-related fatigue: a randomized, double-blind trial, N07C2. Journal of the National Cancer Institute, 105(16), 1230–1238. doi:10.1093/jnci/djt181
- Bell, L., Whyte, A., Duysburgh, C., Marzorati, M., Van den Abbeele, P., Le Cozannet, R., Fança-Berthon, P., Fromentin, E., & Williams, C. (2022). A randomized, placebo-controlled trial investigating the acute and chronic benefits of American Ginseng (Cereboost®) on mood and cognition in healthy young adults, including in vitro investigation of gut microbiota changes as a possible mechanism of action. European journal of nutrition, 61(1), 413–428. doi:10.1007/s00394-021-02654-5
- Lyon, M. R., Cline, J. C., Totosy de Zepetnek, J., Shan, J. J., Pang, P., & Benishin, C. (2001). Effect of the herbal extract combination Panax quinquefolium and Ginkgo biloba on attention-deficit hyperactivity disorder: a pilot study. Journal of psychiatry & neuroscience : JPN, 26(3), 221–228.
- Ossoukhova, A., Owen, L., Savage, K., Meyer, M., Ibarra, A., Roller, M., Pipingas, A., Wesnes, K., & Scholey, A. (2015). Improved working memory performance following administration of a single dose of American ginseng (Panax quinquefolius L.) to healthy middle-age adults. Human psychopharmacology, 30(2), 108–122. doi:10.1002/hup.2463
- White, D. J., Camfield, D. A., Ossoukhova, A., Savage, K., Le Cozannet, R., Fança-Berthon, P., & Scholey, A. (2020). Effects of Panax quinquefolius (American ginseng) on the steady state visually evoked potential during cognitive performance. Human psychopharmacology, 35(6), 1–6. doi:10.1002/hup.2756
- Scholey, A., Ossoukhova, A., Owen, L., Ibarra, A., Pipingas, A., He, K., Roller, M., & Stough, C. (2010). Effects of American ginseng (Panax quinquefolius) on neurocognitive function: an acute, randomised, double-blind, placebo-controlled, crossover study. Psychopharmacology, 212(3), 345–356. doi:10.1007/s00213-010-1964-y
- Chen, E. Y., & Hui, C. L. (2012). HT1001, a proprietary North American ginseng extract, improves working memory in schizophrenia: a double-blind, placebo-controlled study. Phytotherapy research : PTR, 26(8), 1166–1172. doi:10.1002/ptr.3700
- Barton, D. L., Soori, G. S., Bauer, B. A., Sloan, J. A., Johnson, P. A., Figueras, C., Duane, S., Mattar, B., Liu, H., Atherton, P. J., Christensen, B., & Loprinzi, C. L. (2010). Pilot study of Panax quinquefolius (American ginseng) to improve cancer-related fatigue: a randomized, double-blind, dose-finding evaluation: NCCTG trial N03CA. Supportive care in cancer : official journal of the Multinational Association of Supportive Care in Cancer, 18(2), 179–187. doi:10.1007/s00520-009-0642-2
- Chanana, P., & Kumar, A. (2016). GABA-BZD Receptor Modulating Mechanism of Panax quinquefolius against 72-h Sleep Deprivation Induced Anxiety like Behavior: Possible Roles of Oxidative Stress, Mitochondrial Dysfunction and Neuroinflammation. Frontiers in neuroscience, 10, 84. doi:10.3389/fnins.2016.00084
- Shin, K., Guo, H., Cha, Y., Ban, Y. H., Seo, d., Choi, Y., Kim, T. S., Lee, S. P., Kim, J. C., Choi, E. K., Yon, J. M., & Kim, Y. B. (2016). Cereboost™, an American ginseng extract, improves cognitive function via up-regulation of choline acetyltransferase expression and neuroprotection. Regulatory toxicology and pharmacology : RTP, 78, 53–58. doi:10.1016/j.yrtph.2016.04.006
- Chatterjee, M., Verma, P., & Palit, G. (2010). Comparative evaluation of Bacopa monniera and Panax quniquefolium in experimental anxiety and depressive models in mice. Indian journal of experimental biology, 48(3), 306–313.
- Best, T., Clarke, C., Nuzum, N., & Teo, W. P. (2021). Acute effects of combined Bacopa, American ginseng and whole coffee fruit on working memory and cerebral haemodynamic response of the prefrontal cortex: a double-blind, placebo-controlled study. Nutritional neuroscience, 24(11), 873–884. doi:10.1080/1028415X.2019.1690288
- Yang, L., Hou, A., Zhang, J., Wang, S., Man, W., Yu, H., Zheng, S., Wang, X., Liu, S., & Jiang, H. (2020). Panacis Quinquefolii Radix: A Review of the Botany, Phytochemistry, Quality Control, Pharmacology, Toxicology and Industrial Applications Research Progress. Frontiers in pharmacology, 11, 602092. doi:10.3389/fphar.2020.602092
- Yang, L., Hou, A., Zhang, J., Wang, S., Man, W., Yu, H., Zheng, S., Wang, X., Liu, S., & Jiang, H. (2020). Panacis Quinquefolii Radix: A Review of the Botany, Phytochemistry, Quality Control, Pharmacology, Toxicology and Industrial Applications Research Progress. Frontiers in pharmacology, 11, 602092. doi:10.3389/fphar.2020.602092
- Szczuka, D., Nowak, A., Zakłos-Szyda, M., Kochan, E., Szymańska, G., Motyl, I., & Blasiak, J. (2019). American Ginseng (Panax quinquefolium L.) as a Source of Bioactive Phytochemicals with Pro-Health Properties. Nutrients, 11(5), 1041. doi:10.3390/nu1105104
Rhodiola Rosea - Ma, G. P., Zheng, Q., Xu, M. B., Zhou, X. L., Lu, L., Li, Z. X., & Zheng, G. Q. (2018). Rhodiola rosea L. Improves Learning and Memory Function: Preclinical Evidence and Possible Mechanisms. Frontiers in pharmacology, 9, 1415. doi:10.3389/fphar.2018.01415
- Petkov, V. D., Yonkov, D., Mosharoff, A., Kambourova, T., Alova, L., Petkov, V. V., & Todorov, I. (1986). Effects of alcohol aqueous extract from Rhodiola rosea L. roots on learning and memory. Acta physiologica et pharmacologica Bulgarica, 12(1), 3–16.
- Cropley, M., Banks, A. P., & Boyle, J. (2015). The Effects of Rhodiola rosea L. Extract on Anxiety, Stress, Cognition and Other Mood Symptoms. Phytotherapy research : PTR, 29(12), 1934–1939. doi:10.1002/ptr.5486
- Darbinyan, V., Kteyan, A., Panossian, A., Gabrielian, E., Wikman, G., & Wagner, H. (2000). Rhodiola rosea in stress induced fatigue--a double blind cross-over study of a standardized extract SHR-5 with a repeated low-dose regimen on the mental performance of healthy physicians during night duty. Phytomedicine : international journal of phytotherapy and phytopharmacology, 7(5), 365–371. doi:10.1016/S0944-7113(00)80055-0
- Zotova, M.I. (1965) The effect of Rhodiola rosea extract on mental working activity in man. In: Collection of Reports at 3rd Scientific Conference of Physiologists. Biochemists and Pharmacologists of Western Siberia, Tomsk, 298-299.
- Pogorelyĭ, V. E., & Makarova, L. M. (2002). Ekstrakt rodioly rozovoĭ pri profilaktike ishemicheskikh narusheniĭ mozgovogo krovoobrashcheniia [Rhodiola rosea extract for prophylaxis of ischemic cerebral circulation disorder]. Eksperimental'naia i klinicheskaia farmakologiia, 65(4), 19–22.
- Chen, Y., Tang, M., Yuan, S., Fu, S., Li, Y., Li, Y., Wang, Q., Cao, Y., Liu, L., & Zhang, Q. (2022). Rhodiola rosea: A Therapeutic Candidate on Cardiovascular Diseases. Oxidative medicine and cellular longevity, 2022, 1348795. doi: 10.1155/2022/1348795
- Tian, Z., Li, Y., Wang, G., Wang, J., & Zhang, Y. (2020). Therapeutic Effects of Salidroside on Cognitive Ability in Rats with Experimental Vascular Dementia. Bulletin of experimental biology and medicine, 169(1), 35–39. doi: 10.1007/s10517-020-04818-5
- Yan, Z. Q., Chen, J., Xing, G. X., Huang, J. G., Hou, X. H., & Zhang, Y. (2015). Salidroside prevents cognitive impairment induced by chronic cerebral hypoperfusion in rats. The Journal of international medical research, 43(3), 402–411. doi: 10.1177/0300060514566648
- Länge, R. (2012). Assessment report on Rhodiola rosea L., rhizoma et radix, Based on Article 16d(1), Article 16f and Article 16h of Directive 2001/83/EC as amended (traditional use). European Medicines Agency. https://www.ema.europa.eu/en/documents/herbal-report/final-assessment-report-rhodiola-rosea-first-version_en.pdf
- Perfumi, M., & Mattioli, L. (2007). Adaptogenic and central nervous system effects of single doses of 3% rosavin and 1% salidroside Rhodiola rosea L. extract in mice. Phytotherapy research : PTR, 21(1), 37–43. doi: 10.1002/ptr.2013
- Zhong, Z., Han, J., Zhang, J., Xiao, Q., Hu, J., & Chen, L. (2018). Pharmacological activities, mechanisms of action, and safety of salidroside in the central nervous system. Drug design, development and therapy, 12, 1479–1489. doi: 10.2147/DDDT.S160776
- Panossian, A., & Wikman, G. (2010). Effects of Adaptogens on the Central Nervous System and the Molecular Mechanisms Associated with Their Stress-Protective Activity. Pharmaceuticals (Basel, Switzerland), 3(1), 188–224. doi: 10.3390/ph3010188
- Chen, Q. G., Zeng, Y. S., Qu, Z. Q., Tang, J. Y., Qin, Y. J., Chung, P., Wong, R., & Hägg, U. (2009). The effects of Rhodiola rosea extract on 5-HT level, cell proliferation and quantity of neurons at cerebral hippocampus of depressive rats. Phytomedicine : international journal of phytotherapy and phytopharmacology, 16(9), 830–838. doi: 10.1016/j.phymed.2009.03.011
- van Diermen, D., Marston, A., Bravo, J., Reist, M., Carrupt, P. A., & Hostettmann, K. (2009). Monoamine oxidase inhibition by Rhodiola rosea L. roots. Journal of ethnopharmacology, 122(2), 397–401. doi: 10.1016/j.jep.2009.01.007
- Johnson, K. (2016, August 19). Before Steroids, Russians Secretly Studied Herbs. National Geographic. https://www.nationalgeographic.com/culture/article/long-before-doping-scandals--russians-were-studying-performance-
- Spasov, A. A., Wikman, G. K., Mandrikov, V. B., Mironova, I. A., & Neumoin, V. V. (2000). A double-blind, placebo-controlled pilot study of the stimulating and adaptogenic effect of Rhodiola rosea SHR-5 extract on the fatigue of students caused by stress during an examination period with a repeated low-dose regimen. Phytomedicine : international journal of phytotherapy and phytopharmacology, 7(2), 85–89. doi:10.1016/S0944-7113(00)80078-1
- Shevtsov, V. A., Zholus, B. I., Shervarly, V. I., Vol'skij, V. B., Korovin, Y. P., Khristich, M. P., Roslyakova, N. A., & Wikman, G. (2003). A randomized trial of two different doses of a SHR-5 Rhodiola rosea extract versus placebo and control of capacity for mental work. Phytomedicine : international journal of phytotherapy and phytopharmacology, 10(2-3), 95–105. doi:10.1078/094471103321659780
- Duncan, M. J., & Clarke, N. D. (2014). The Effect of Acute Rhodiola rosea Ingestion on Exercise Heart Rate, Substrate Utilisation, Mood State, and Perceptions of Exertion, Arousal, and Pleasure/Displeasure in Active Men. Journal of sports medicine (Hindawi Publishing Corporation), 2014, 563043. doi: 10.1155/2014/563043
- Ishaque, S., Shamseer, L., Bukutu, C., & Vohra, S. (2012). Rhodiola rosea for physical and mental fatigue: a systematic review. BMC complementary and alternative medicine, 12, 70. doi:10.1186/1472-6882-12-70
- Panossian, A., Wikman, G., & Sarris, J. (2010). Rosenroot (Rhodiola rosea): Traditional use, chemical composition, pharmacology and clinical efficacy. Phytomedicine, 17(7), 481–493. doi:10.1016/j.phymed.2010.02.002
- Panossian A, Wagner H. Adaptogens. A review of their history, biological activity, and clinical benefits. HerbalGram. 2011;90:52‐63.
- Anghelescu, I. G., Edwards, D., Seifritz, E., & Kasper, S. (2018). Stress management and the role of Rhodiola rosea: a review. International journal of psychiatry in clinical practice, 22(4), 242–252. doi:10.1080/13651501.2017.1417442
- Kelly G. S. (2001). Rhodiola rosea: a possible plant adaptogen. Alternative medicine review : a journal of clinical therapeutic, 6(3), 293–302.
- Olsson, E. M., von Schéele, B., & Panossian, A. G. (2009). A randomised, double-blind, placebo-controlled, parallel-group study of the standardised extract shr-5 of the roots of Rhodiola rosea in the treatment of subjects with stress-related fatigue. Planta medica, 75(2), 105–112. doi:10.1055/s-0028-1088346
- Ross S. M. (2014). Rhodiola rosea (SHR-5), Part I: a proprietary root extract of Rhodiola rosea is found to be effective in the treatment of stress-related fatigue. Holistic nursing practice, 28(2), 149–154. doi:10.1097/HNP.0000000000000014
- Ha, Z., Zhu, Y., Zhang, X., Cui, J., Zhang, S., Ma, Y., Wang, W., & Jian, X. (2002). Zhonghua jie he he hu xi za zhi = Zhonghua jiehe he huxi zazhi =/ [The effect of rhodiola and acetazolamide on the sleep architecture and blood oxygen saturation in men living at high altitude] Chinese journal of tuberculosis and respiratory diseases, 25(9), 527–530.
- Darbinyan, V., Aslanyan, G., Amroyan, E., Gabrielyan, E., Malmström, C., & Panossian, A. (2007). Clinical trial of Rhodiola rosea L. extract SHR-5 in the treatment of mild to moderate depression. Nordic journal of psychiatry, 61(5), 343–348. doi:10.1080/08039480701643290
- Hao, Y. F., Luo, T., Lu, Z. Y., Shen, C. Y., & Jiang, J. G. (2021). Targets and underlying mechanisms related to the sedative and hypnotic activities of saponins from Rhodiola rosea L. (crassulaceae). Food & function, 12(21), 10589–10601. doi: 10.1039/d1fo01178b
- Fintelmann, V., & Gruenwald, J. (2007). Efficacy and tolerability of aRhodiola rosea extract in adults with physical and cognitive deficiencies. Advances in Therapy, 24(4), 929–939. doi:10.1007/bf02849986
- Pomari, E., Stefanon, B., & Colitti, M. (2015). Effects of Two Different Rhodiola rosea Extracts on Primary Human Visceral Adipocytes. Molecules (Basel, Switzerland), 20(5), 8409–8428. doi: 10.3390/molecules20058409
- Xu, Y., Jiang, H., Sun, C., Adu-Frimpong, M., Deng, W., Yu, J., & Xu, X. (2018). Antioxidant and hepatoprotective effects of purified Rhodiola rosea polysaccharides. International journal of biological macromolecules, 117, 167–178. doi: 10.1016/j.ijbiomac.2018.05.168
- Yuan, Y., Wu, X., Zhang, X., Hong, Y., & Yan, H. (2019). Ameliorative effect of salidroside from Rhodiola Rosea L. on the gut microbiota subject to furan-induced liver injury in a mouse model. Food and chemical toxicology : an international journal published for the British Industrial Biological Research Association, 125, 333–340. doi: 10.1016/j.fct.2019.01.007
- Wen, S. Y., Chen, Y. Y., Lu, J. X., Liang, Q. Q., Shi, H., Wu, Q., Yao, Z. H., Zhu, Y., & Jiang, M. M. (2020). Modulation of hepatic lipidome by rhodioloside in high-fat diet fed apolipoprotein E knockout mice. Phytomedicine : international journal of phytotherapy and phytopharmacology, 69, 152690. doi: 10.1016/j.phymed.2018.09.225
- Abidov, M., Crendal, F., Grachev, S., Seifulla, R., & Ziegenfuss, T. (2003). Effect of extracts from Rhodiola rosea and Rhodiola crenulata (Crassulaceae) roots on ATP content in mitochondria of skeletal muscles. Bulletin of experimental biology and medicine, 136(6), 585–587. doi:10.1023/b:bebm.0000020211.24779.15
- Lee, F. T., Kuo, T. Y., Liou, S. Y., & Chien, C. T. (2009). Chronic Rhodiola rosea extract supplementation enforces exhaustive swimming tolerance. The American journal of Chinese medicine, 37(3), 557–572. doi: 10.1142/S0192415X09007053
- Abidov, M., Grachev, S., Seifulla, R. D., & Ziegenfuss, T. N. (2004). Extract of Rhodiola rosea radix reduces the level of C-reactive protein and creatinine kinase in the blood. Bulletin of experimental biology and medicine, 138(1), 63–64. doi: 10.1023/b:bebm.0000046940.45382.53
- De Bock, K., Eijnde, B. O., Ramaekers, M., & Hespel, P. (2004). Acute Rhodiola rosea intake can improve endurance exercise performance. International journal of sport nutrition and exercise metabolism, 14(3), 298–307. doi: 10.1123/ijsnem.14.3.298
- Jówko, E., Sadowski, J., Długołęcka, B., Gierczuk, D., Opaszowski, B., & Cieśliński, I. (2018). Effects of Rhodiola rosea supplementation on mental performance, physical capacity, and oxidative stress biomarkers in healthy men. Journal of sport and health science, 7(4), 473–480. doi: 10.1016/j.jshs.2016.05.005
Bacopa monnieri - Shinomol, G. K., Muralidhara, & Bharath, M. M. (2011). Exploring the Role of “Brahmi” (Bacopa monnieri and Centella asiatica) in Brain Function and Therapy. Recent patents on endocrine, metabolic & immune drug discovery, 5(1), 33–49. doi: 10.2174/187221411794351833
- Rastogi, M., Ojha, R. P., Prabu, P. C., Devi, B. P., Agrawal, A., & Dubey, G. P. (2012). Prevention of age-associated neurodegeneration and promotion of healthy brain ageing in female Wistar rats by long term use of bacosides. Biogerontology, 13(2), 183–195. doi: 10.1007/s10522-011-9367-y
- Holcomb, L. A., Dhanasekaran, M., Hitt, A. R., Young, K. A., Riggs, M., & Manyam, B. V. (2006). Bacopa monniera extract reduces amyloid levels in PSAPP mice. Journal of Alzheimer's disease : JAD, 9(3), 243–251. doi:10.3233/jad-2006-9303
- Rastogi, M., Ojha, R. P., Prabu, P. C., Devi, B. P., Agrawal, A., & Dubey, G. P. (2012). Prevention of age-associated neurodegeneration and promotion of healthy brain ageing in female Wistar rats by long term use of bacosides. Biogerontology, 13(2), 183–195. doi:10.1007/s10522-011-9367-y
- Jyoti, A., Sethi, P., & Sharma, D. (2007). Bacopa monniera prevents from aluminium neurotoxicity in the cerebral cortex of rat brain. Journal of ethnopharmacology, 111(1), 56–62. doi: 10.1016/j.jep.2006.10.037
- Jyoti, A., & Sharma, D. (2006). Neuroprotective role of Bacopa monniera extract against aluminium-induced oxidative stress in the hippocampus of rat brain. Neurotoxicology, 27(4), 451–457. doi: 10.1016/j.neuro.2005.12.007
- Khan, R., Krishnakumar, A., & Paulose, C. S. (2008). Decreased glutamate receptor binding and NMDA R1 gene expression in hippocampus of pilocarpine-induced epileptic rats: neuroprotective role of Bacopa monnieri extract. Epilepsy & behavior : E&B, 12(1), 54–60. doi: 10.1016/j.yebeh.2007.09.021
- Singh H. K. (2013). Brain enhancing ingredients from Āyurvedic medicine: quintessential example of Bacopa monniera, a narrative review. Nutrients, 5(2), 478–497. doi: 10.3390/nu5020478
- Singh, R. H., Narsimhamurthy, K., & Singh, G. (2008). Neuronutrient impact of Ayurvedic Rasayana therapy in brain aging. Biogerontology, 9(6), 369–374. doi: 10.1007/s10522-008-9185-z
- Uabundit, N., Wattanathorn, J., Mucimapura, S., & Ingkaninan, K. (2010). Cognitive enhancement and neuroprotective effects of Bacopa monnieri in Alzheimer's disease model. Journal of ethnopharmacology, 127(1), 26–31. doi:10.1016/j.jep.2009.09.056
- Barbhaiya, H.C., Desai, R.P., Saxena, V.S., Pravina, K., Wasim, P., Geetharani, P., Allan, J.J., Venkateshwarlu, K., & Amit, A. (2008). Efficacy and Tolerability of BacoMind®on Memory Improvement in Elderly Participants – A Double Blind Placebo Controlled Study. Journal of Pharmacology and Toxicology, 3, 425-434. doi:10.3923/jpt.2008.425.434
- Dwivedi, S., Nagarajan, R., Hanif, K., Siddiqui, H. H., Nath, C., & Shukla, R. (2013). Standardized Extract of Bacopa monniera Attenuates Okadaic Acid Induced Memory Dysfunction in Rats: Effect on Nrf2 Pathway. Evidence-based complementary and alternative medicine : eCAM, 2013, 294501. doi:10.1155/2013/294501
- Habbu, P., Madagundi, S., Kulkarni, R., Jadav, S., Vanakudri, R., & Kulkarni, V. (2013). Preparation and evaluation of Bacopa–phospholipid complex for antiamnesic activity in rodents. Drug Invention Today, 5(1), 13–21. doi:10.1016/j.dit.2013.02.004
- Kean, J. D., Downey, L. A., & Stough, C. (2016). A systematic review of the Ayurvedic medicinal herb Bacopa monnieri in child and adolescent populations. Complementary therapies in medicine, 29, 56–62. doi:10.1016/j.ctim.2016.09.002
- Morgan, A., & Stevens, J. (2010). Does Bacopa monnieri improve memory performance in older persons? Results of a randomized, placebo-controlled, double-blind trial. Journal of alternative and complementary medicine (New York, N.Y.), 16(7), 753–759. doi:10.1089/acm.2009.0342
- Peth-Nui, T., Wattanathorn, J., Muchimapura, S., Tong-Un, T., Piyavhatkul, N., Rangseekajee, P., Ingkaninan, K., & Vittaya-Areekul, S. (2012). Effects of 12-Week Bacopa monnieri Consumption on Attention, Cognitive Processing, Working Memory, and Functions of Both Cholinergic and Monoaminergic Systems in Healthy Elderly Volunteers. Evidence-based complementary and alternative medicine : eCAM, 2012, 606424. doi:10.1155/2012/606424
- Pravina, K., Ravindra, K. R., Goudar, K. S., Vinod, D. R., Joshua, A. J., Wasim, P., Venkateshwarlu, K., Saxena, V. S., & Amit, A. (2007). Safety evaluation of BacoMind in healthy volunteers: a phase I study. Phytomedicine : international journal of phytotherapy and phytopharmacology, 14(5), 301–308. doi:10.1016/j.phymed.2007.03.010
- Raghav, S., Singh, H., Dalal, P. K., Srivastava, J. S., & Asthana, O. P. (2006). Randomized controlled trial of standardized Bacopa monniera extract in age-associated memory impairment. Indian journal of psychiatry, 48(4), 238–242. doi:10.4103/0019-5545.31555
- Roodenrys, S., Booth, D., Bulzomi, S., Phipps, A., Micallef, C., & Smoker, J. (2002). Chronic effects of Brahmi (Bacopa monnieri) on human memory. Neuropsychopharmacology : official publication of the American College of Neuropsychopharmacology, 27(2), 279–281. doi:10.1016/S0893-133X(01)00419-5
- Saraf, M. K., Prabhakar, S., Khanduja, K. L., & Anand, A. (2011). Bacopa monniera Attenuates Scopolamine-Induced Impairment of Spatial Memory in Mice. Evidence-based complementary and alternative medicine : eCAM, 2011, 236186. doi:10.1093/ecam/neq038
- Charles, P. D., Ambigapathy, G., Geraldine, P., Akbarsha, M. A., & Rajan, K. E. (2011). Bacopa monniera leaf extract up-regulates tryptophan hydroxylase (TPH2) and serotonin transporter (SERT) expression: implications in memory formation. Journal of ethnopharmacology, 134(1), 55–61. doi: 10.1016/j.jep.2010.11.045
- Charoenphon, N., Anandsongvit, N., Kosai, P., Sirisidthi, K., Kangwanrangsan, N., & Jiraungkoorskul, W. (2016). Brahmi (Bacopa monnieri): Up-to-date of memory boosting medicinal plant: A review. Indian journal of agricultural research, 50, 1-7.
- Peth-Nui, T., Wattanathorn, J., Muchimapura, S., Tong-Un, T., Piyavhatkul, N., Rangseekajee, P., Ingkaninan, K., & Vittaya-Areekul, S. (2012). Effects of 12-Week Bacopa monnieri Consumption on Attention, Cognitive Processing, Working Memory, and Functions of Both Cholinergic and Monoaminergic Systems in Healthy Elderly Volunteers. Evidence-based complementary and alternative medicine : eCAM, 2012, 606424. doi: 10.1155/2012/606424
- Russo, A., & Borrelli, F. (2005). Bacopa monniera, a reputed nootropic plant: an overview. Phytomedicine : international journal of phytotherapy and phytopharmacology, 12(4), 305–317. doi: 10.1016/j.phymed.2003.12.008
- Calabrese, C., Gregory, W. L., Leo, M., Kraemer, D., Bone, K., & Oken, B. (2008). Effects of a standardized Bacopa monnieri extract on cognitive performance, anxiety, and depression in the elderly: a randomized, double-blind, placebo-controlled trial. Journal of alternative and complementary medicine (New York, N.Y.), 14(6), 707–713. doi:10.1089/acm.2008.0018
- Stough, C., Downey, L. A., Lloyd, J., Silber, B., Redman, S., Hutchison, C., Wesnes, K., & Nathan, P. J. (2008). Examining the nootropic effects of a special extract of Bacopa monniera on human cognitive functioning: 90 day double-blind placebo-controlled randomized trial. Phytotherapy research : PTR, 22(12), 1629–1634. doi:10.1002/ptr.2537
- Cicero, A. F., Bove, M., Colletti, A., Rizzo, M., Fogacci, F., Giovannini, M., & Borghi, C. (2017). Short-Term Impact of a Combined Nutraceutical on Cognitive Function, Perceived Stress and Depression in Young Elderly with Cognitive Impairment: A Pilot, Double-Blind, Randomized Clinical Trial. The journal of prevention of Alzheimer's disease, 4(1), 12–15. doi:10.14283/jpad.2016.10
- Dimpfel, W., Schombert, L., Biller, A. (2016) Psychophysiological Effects of Sideritis and Bacopa Extract and Three Combinations Thereof—A Quantitative EEG Study in Subjects Suffering from Mild Cognitive Impairment (MCI). Advances in Alzheimer's Disease. 05. 1-22. doi:10.4236/aad.2016.51001
- Downey, L. A., Kean, J., Nemeh, F., Lau, A., Poll, A., Gregory, R., Murray, M., Rourke, J., Patak, B., Pase, M. P., Zangara, A., Lomas, J., Scholey, A., & Stough, C. (2013). An acute, double-blind, placebo-controlled crossover study of 320 mg and 640 mg doses of a special extract of Bacopa monnieri (CDRI 08) on sustained cognitive performance. Phytotherapy research : PTR, 27(9), 1407–1413. doi:10.1002/ptr.4864
- Khan, M. B., Ahmad, M., Ahmad, S., Ishrat, T., Vaibhav, K., Khuwaja, G., & Islam, F. (2015). Bacopa monniera ameliorates cognitive impairment and neurodegeneration induced by intracerebroventricular-streptozotocin in rat: behavioral, biochemical, immunohistochemical and histopathological evidences. Metabolic brain disease, 30(1), 115–127. doi:10.1007/s11011-014-9593-5
- Kongkeaw, C., Dilokthornsakul, P., Thanarangsarit, P., Limpeanchob, N., & Norman Scholfield, C. (2014). Meta-analysis of randomized controlled trials on cognitive effects of Bacopa monnieri extract. Journal of ethnopharmacology, 151(1), 528–535. doi:10.1016/j.jep.2013.11.008
- Kumar, N., Abichandani, L. G., Thawani, V., Gharpure, K. J., Naidu, M. U., & Venkat Ramana, G. (2016). Efficacy of Standardized Extract of Bacopa monnieri (Bacognize®) on Cognitive Functions of Medical Students: A Six-Week, Randomized Placebo-Controlled Trial. Evidence-based complementary and alternative medicine : eCAM, 2016, 4103423. doi:10.1155/2016/4103423
- Pase, M. P., Kean, J., Sarris, J., Neale, C., Scholey, A. B., & Stough, C. (2012). The cognitive-enhancing effects of Bacopa monnieri: a systematic review of randomized, controlled human clinical trials. Journal of alternative and complementary medicine (New York, N.Y.), 18(7), 647–652. doi:10.1089/acm.2011.0367
- Prabhakar, S., Vishnu, V. Y., Modi, M., Mohanty, M., Sharma, A., Medhi, B., Mittal, B. R., Khandelwal, N., Goyal, M. K., Lal, V., Singla, R., Kansal, A., & Avasthi, A. (2020). Efficacy of Bacopa Monnieri (Brahmi) and Donepezil in Alzheimer's Disease and Mild Cognitive Impairment: A Randomized Double-Blind Parallel Phase 2b Study. Annals of Indian Academy of Neurology, 23(6), 767–773. doi:10.4103/aian.AIAN_610_19
- Sharma, R., Chaturvedi, C., & Tewari, P. (1987) Efficacy of Bacopa monniera in revitalizing intellectual functions in children. J Res Edu Ind Med. 1987;1:12.
- Stough, C., Lloyd, J., Clarke, J., Downey, L. A., Hutchison, C. W., Rodgers, T., & Nathan, P. J. (2001). The chronic effects of an extract of Bacopa monniera (Brahmi) on cognitive function in healthy human subjects. Psychopharmacology, 156(4), 481–484. doi:10.1007/s002130100815
- Usha, P., Wasim, P., Joshua, J., Geetharani, P., Murali, B., Mayachari, A., Venkateshwarlu, K., Saxena, V.S., Deepak, M., & Amit, A. (2008). BacoMind®: A Cognitive Enhancer in Children Requiring Individual Education Programme. Journal of Pharmacology and Toxicology, 3, 302-310. doi:10.3923/jpt.2008.302.310
- Kamkaew, N., Norman Scholfield, C., Ingkaninan, K., Taepavarapruk, N., & Chootip, K. (2013). Bacopa monnieri increases cerebral blood flow in rat independent of blood pressure. Phytotherapy research : PTR, 27(1), 135–138. doi: 10.1002/ptr.4685
- Aguiar, S., & Borowski, T. (2013). Neuropharmacological review of the nootropic herb Bacopa monnieri. Rejuvenation research, 16(4), 313–326. doi: 10.1089/rej.2013.1431
- Srimachai, S., Devaux, S., Demougeot, C., Kumphune, S., Ullrich, N. D., Niggli, E., Ingkaninan, K., Kamkaew, N., Scholfield, C. N., Tapechum, S., & Chootip, K. (2017). Bacopa monnieri extract increases rat coronary flow and protects against myocardial ischemia/reperfusion injury. BMC complementary and alternative medicine, 17(1), 117. doi: 10.1186/s12906-017-1637-z
- Chen, Z., & Yan, Y. (2017). Pharmaceutical composition and drug effect of synthetic Bacopa monnieri L. health promoting agent from the perspective of resistance fatigue. Pakistan journal of pharmaceutical sciences, 30(5(Special)), 1867–1874.
- Ven Murthy, M. R., Ranjekar, P. K., Ramassamy, C., & Deshpande, M. (2010). Scientific basis for the use of Indian ayurvedic medicinal plants in the treatment of neurodegenerative disorders: ashwagandha. Central nervous system agents in medicinal chemistry, 10(3), 238–246. doi: 10.2174/1871524911006030238
- Vollala, V. R., Upadhya, S., & Nayak, S. (2011). Enhanced dendritic arborization of hippocampal CA3 neurons by Bacopa monniera extract treatment in adult rats. Romanian journal of morphology and embryology = Revue roumaine de morphologie et embryologie, 52(3), 879–886.
- Vollala, V. R., Upadhya, S., & Nayak, S. (2011). Enhanced dendritic arborization of amygdala neurons during growth spurt periods in rats orally intubated with Bacopa monniera extract. Anatomical science international, 86(4), 179–188. doi: 10.1007/s12565-011-0104-z
- Vollala, V. R., Upadhya, S., & Nayak, S. (2011). Enhancement of basolateral amygdaloid neuronal dendritic arborization following Bacopa monniera extract treatment in adult rats. Clinics (Sao Paulo, Brazil), 66(4), 663–671. doi: 10.1590/s1807-59322011000400023
- Bhattacharya, S. K., Bhattacharya, A., Kumar, A., & Ghosal, S. (2000). Antioxidant activity of Bacopa monniera in rat frontal cortex, striatum and hippocampus. Phytotherapy research : PTR, 14(3), 174–179. doi: 10.1002/(sici)1099-1573(200005)14:3<174::aid-ptr624>3.0.co;2-o
- Percário, S., da Silva Barbosa, A., Varela, E., Gomes, A., Ferreira, M., de Nazaré Araújo Moreira, T., & Dolabela, M. F. (2020). Oxidative Stress in Parkinson's Disease: Potential Benefits of Antioxidant Supplementation. Oxidative medicine and cellular longevity, 2020, 2360872. doi: 10.1155/2020/2360872
- Biswas, SK. (2012). Evaluation of antinociceptive and antioxidant activities of whole plant extrakt of Bacopa monnieri. Res J Med Plant 2012; 6:607-14.
- Tripathi, Y. B., Chaurasia, S., Tripathi, E., Upadhyay, A., & Dubey, G. P. (1996). Bacopa monniera Linn. as an antioxidant: mechanism of action. Indian journal of experimental biology, 34(6), 523–526.
- Simpson, T., Pase, M., & Stough, C. (2015). Bacopa monnieri as an Antioxidant Therapy to Reduce Oxidative Stress in the Aging Brain. Evidence-based complementary and alternative medicine : eCAM, 2015, 615384. doi: 10.1155/2015/615384
- Benson, S., Downey, L. A., Stough, C., Wetherell, M., Zangara, A., & Scholey, A. (2014). An acute, double-blind, placebo-controlled cross-over study of 320 mg and 640 mg doses of Bacopa monnieri (CDRI 08) on multitasking stress reactivity and mood. Phytotherapy research : PTR, 28(4), 551–559. doi:10.1002/ptr.5029
- Sheikh, N., Ahmad, A., Siripurapu, K. B., Kuchibhotla, V. K., Singh, S., & Palit, G. (2007). Effect of Bacopa monniera on stress induced changes in plasma corticosterone and brain monoamines in rats. Journal of ethnopharmacology, 111(3), 671–676. doi: 10.1016/j.jep.2007.01.025
- Chowdhuri, D. K., Parmar, D., Kakkar, P., Shukla, R., Seth, P. K., & Srimal, R. C. (2002). Antistress effects of bacosides of Bacopa monnieri: modulation of Hsp70 expression, superoxide dismutase and cytochrome P450 activity in rat brain. Phytotherapy research : PTR, 16(7), 639–645. doi: 10.1002/ptr.1023
- Shetty S.K., Rao P.N., U S. et al. (2020). The effect of Brahmi (Bacopa monnieri (L.) Pennell) on depression, anxiety and stress during Covid-19. European Journal of Integrative Medicine. Vol. 48:101898-101898. doi: 10.1016/j.eujim.2021.101898
- Lopresti, A. L., Smith, S. J., Ali, S., Metse, A. P., Kalns, J., & Drummond, P. D. (2021). Effects of a Bacopa monnieri extract (Bacognize®) on stress, fatigue, quality of life and sleep in adults with self-reported poor sleep: A randomised, double-blind, placebo-controlled study. Journal of Functional Foods, 85, 104671. doi:10.1016/j.jff.2021.104671
- Kean, J. D., Downey, L. A., Sarris, J., Kaufman, J., Zangara, A., & Stough, C. (2022). Effects of Bacopa monnieri (CDRI 08®) in a population of males exhibiting inattention and hyperactivity aged 6 to 14 years: A randomized, double-blind, placebo-controlled trial. Phytotherapy Research, 36( 2), 996– 1012. doi: 10.1002/ptr.7372
- Lewis, J. E., Poles, J., Shaw, D. P., Karhu, E., Khan, S. A., Lyons, A. E., Sacco, S. B., & McDaniel, H. R. (2021). The effects of twenty-one nutrients and phytonutrients on cognitive function: A narrative review. Journal of clinical and translational research, 7(4), 575–620.
Uwolnij pełen potencjał swojego umysłu. Naukowo.


LEPSZA PAMIĘĆ

WYDŁUŻONA KONCENTRACJA

SZYBSZE MYŚLENIE



© Rozwojowiec 2012-2022
Rozwojowiec Sp. z o.o. z siedzibą przy ul. Romana Dmowskiego 3/9 50-203 Wrocław, Sąd rejonowy dla Wrocławia Fabrycznej we Wrocławiu, VI wydział gospodarczy KRS, KRS 0000943812, Kapitał założycielski 100 000,00 PLN, NIP 8982272217, REGON 520854136









